Alectinib
アレクチニブ (アレセンサ®)
Alectinib:アレクチニブ(アレセンサ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 300mg2錠2x | 連日内服 | Day 1~ |
その他
| ALK融合遺伝子陽性の切除不能な進行・再発のNSCLCに適応を有する。 |
| 開始前に間質性肺炎、 肝機能障害、 QT延長がないことを確認する。 |
| 連日内服、 PDまで継続する。 |
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
💊 アレクチニブ (アレセンサ®)
*中外製薬株式会社の外部サイトへ遷移します
用法・用量
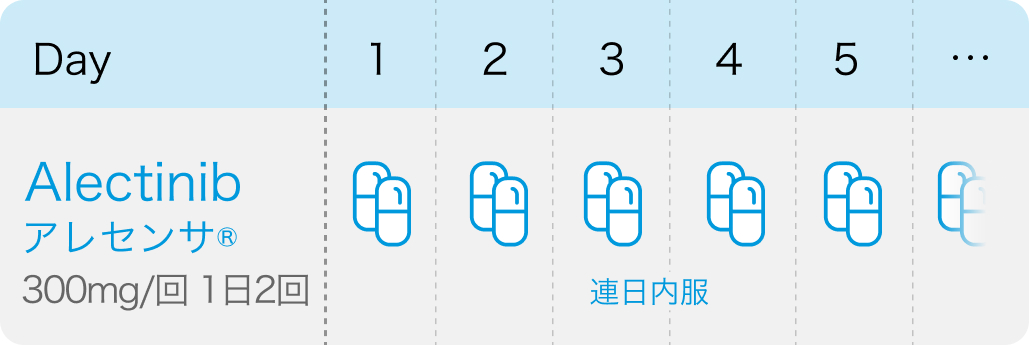
ALK融合遺伝子陽性の切除不能な進行・再発のNSCLC: 成人には1回300mgを1日2回経口投与¹⁾
>再発又は難治性のALK陽性ALCLの適応についてはこちら
減量・中止する場合の用量
減量設定なし、忍容性が得られない場合は中止¹⁾
休薬・中止基準
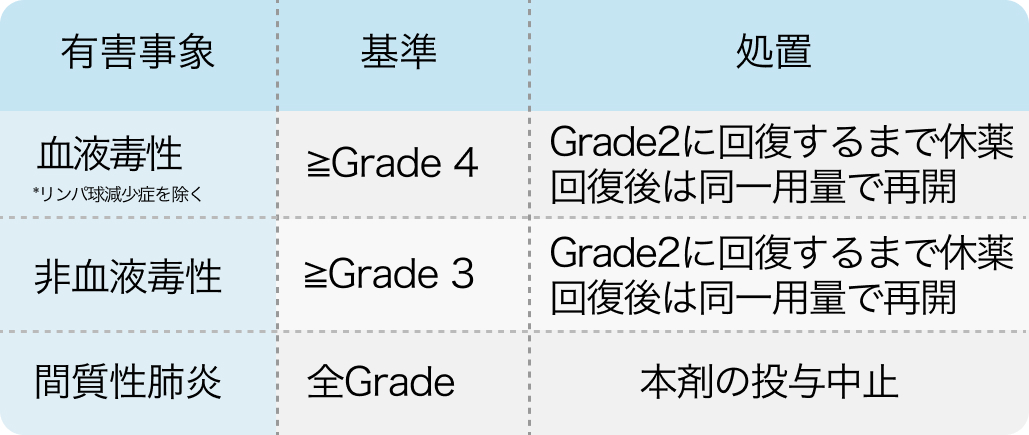
間質性肺疾患が疑われる場合には、 直ちに休薬する。 その後CT検査等による適切な検査を実施し、 間質性肺疾患と診断された場合にはGradeに関わらず投与を中止する¹⁾。
特徴と注意点
国内で2番目に承認された第2世代ALK阻害薬。 ALK陽性進行NSCLCは、 NSCLCの3~5%で認められ、 特に若年者や非喫煙者に多い²⁾。
>再発又は難治性のALK陽性ALCLの適応についてはこちら
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
肺癌診療ガイドライン2023の推奨³⁾
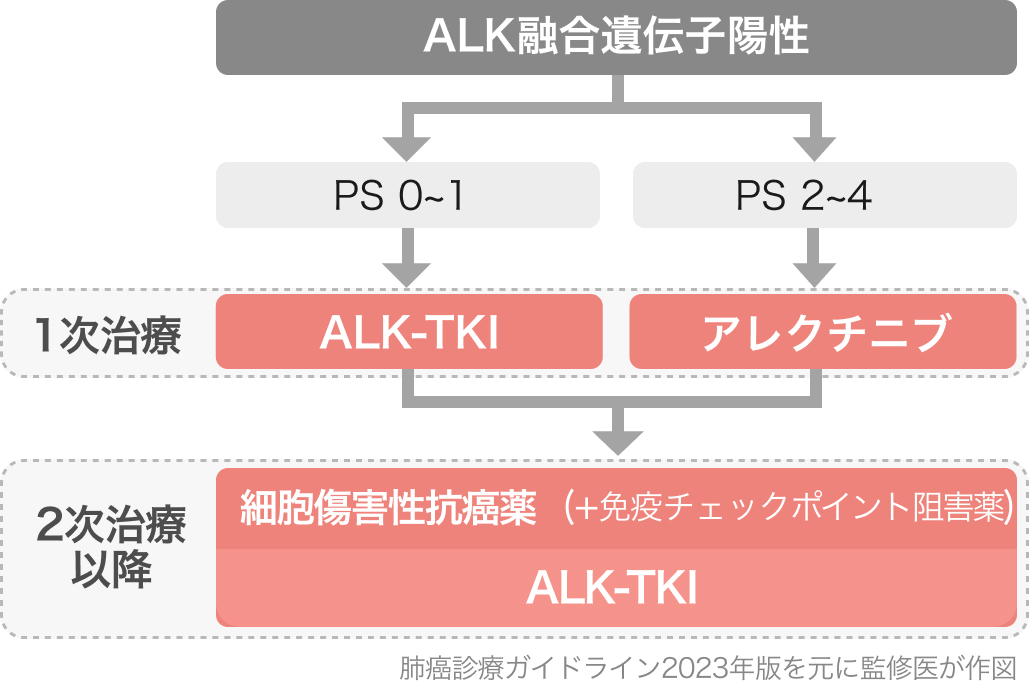
PS 0-1の場合、 1次治療でALK-TKIを推奨・提案 (以下薬剤について記載あり)。
・ アレクチニブ (Alectinib) [推奨 1A]
・ ブリグチニブ (Brigatinib) [提案 2B]
・ ロルラチニブ (Lorlatinib) [提案 2B]
PS 2-4の場合,1次治療とでアレクチニブ単剤療法を行うよう推奨[1C]。
・ アレクチニブ (Alectinib) [推奨 1C]
アレクチニブ耐性または増悪後の症例に対して、 ALK-TKI単剤療法 (ブリグチニブ、 ロルラチニブ、 セリチニブ) を行うよう提案[2C]。
・ アレクチニブ (Alectinib) [提案 2C]
・ ロルラチニブ (Lorlatinib) [提案 2C]
・ セリチニブ (Ceritinib) [提案 2C]
主要な臨床試験 (PS 0~1)
📊 ALEX試験 [海外]⁴⁾
NEJM. 2017 Aug 31;377(9):829-38.
国際共同無作為化非盲検の第3相試験
前治療歴のないALK陽性進行期NSCLC患者を対象に、 アレクチニブ (600mg 1日2回) とクリゾチニブ (250mg 1日2回)を比較した。 2014年8月~2016年1月の間、 98施設より303例が登録され、 アレクチニブ群 152例、 クリゾチニブ群 151例が無作為に割り付けられた。
無増悪生存期間 [主要評価項目]
- アレクチニブ群 未到達 (95%CI 17.7−NA)
- クリゾチニブ群 11.1ヶ月 (9.1−13.1)
HR 0.47 (0.34−0.65、 P<0.001)
奏功割合
- アレクチニブ群 82.9% (76.0−88.5)
- クリゾチニブ群 75.5% (67.8−82.1)
📊 J-ALEX試験 [国内]⁵⁾⁶⁾
Lancet. 2017 Jul 1;390(10089):29-39. / Lung Cancer. 2020 Jan;139:195-199.
日本人患者対象の第3相試験
日本人進行ALK遺伝子転座陽性非小細胞肺癌患者を対象に、 アレクチニブ (300mg 1日2回) とクリゾチニブ (250mg 1日2回) を比較した。 2013年11月18日~2015年8月4日の間に207例が登録され、 アレクチニブ群 103例、 クリゾチニブ群 104例が無作為に割り付けられた。
無増悪生存期間 [主要評価項目 最終解析]
- アレクチニブ群 34.1ヶ月 (20.3−NA)
- クリゾチニブ群 10.2ヶ月 (8.2-12.0)
HR 0.37 (0.26-0.52、 P<0.001)
奏功割合
- アレクチニブ群 92% (85.6-97.5)
- クリゾチニブ群 79% (70.5-87.3)
主要な臨床試験 (PS 2~4)
📊LOGiK1401試験 [国内]⁷⁾⁸⁾
ALK融合遺伝子陽性のPS不良患者を対象として、 アレクチニブ単剤療法の有効性および安全性を評価した第Ⅱ相試験。 対象患者は計18例 (PS2: 12例、 PS3: 5例、 PS4: 1例)。 有効性は以下のとおりで、 安全性に大きな問題はなかった。
- ORR (主要評価項目) 72.2%
- 無増悪生存期間 [最終解析] 16.2カ月
- OS中央値 [最終解析] 30.3カ月
- PSの改善 83.3%の患者で認めた
参考文献
1) 中外製薬株式会社 「アレセンサ®適正使用ガイド」 (2020年2月改訂) [最終確認 2024/03/02]
2) 日本肺癌学会バイオマーカー委員会. 肺癌患者におけるALK融合遺伝子検査の手引き第4.0版
3) 日本肺癌学会. 肺癌診療ガイドライン−悪性胸膜中皮腫・ 胸腺腫瘍含む−2023年版
最終更新日:2024年3月2日
HOKUTO編集部医師監修
Alectinib
Alectinib:アレクチニブ(アレセンサ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 300mg2錠2x | 連日内服 | Day 1~ |
その他
| ALK融合遺伝子陽性の切除不能な進行・再発のNSCLCに適応を有する。 |
| 開始前に間質性肺炎、 肝機能障害、 QT延長がないことを確認する。 |
| 連日内服、 PDまで継続する。 |
概要
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
💊 アレクチニブ (アレセンサ®)
*中外製薬株式会社の外部サイトへ遷移します
用法・用量

ALK融合遺伝子陽性の切除不能な進行・再発のNSCLC: 成人には1回300mgを1日2回経口投与¹⁾
>再発又は難治性のALK陽性ALCLの適応についてはこちら
減量・中止する場合の用量
減量設定なし、忍容性が得られない場合は中止¹⁾
休薬・中止基準

間質性肺疾患が疑われる場合には、 直ちに休薬する。 その後CT検査等による適切な検査を実施し、 間質性肺疾患と診断された場合にはGradeに関わらず投与を中止する¹⁾。
特徴と注意点
国内で2番目に承認された第2世代ALK阻害薬。 ALK陽性進行NSCLCは、 NSCLCの3~5%で認められ、 特に若年者や非喫煙者に多い²⁾。
>再発又は難治性のALK陽性ALCLの適応についてはこちら
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
肺癌診療ガイドライン2023の推奨³⁾

PS 0-1の場合、 1次治療でALK-TKIを推奨・提案 (以下薬剤について記載あり)。
・ アレクチニブ (Alectinib) [推奨 1A]
・ ブリグチニブ (Brigatinib) [提案 2B]
・ ロルラチニブ (Lorlatinib) [提案 2B]
PS 2-4の場合,1次治療とでアレクチニブ単剤療法を行うよう推奨[1C]。
・ アレクチニブ (Alectinib) [推奨 1C]
アレクチニブ耐性または増悪後の症例に対して、 ALK-TKI単剤療法 (ブリグチニブ、 ロルラチニブ、 セリチニブ) を行うよう提案[2C]。
・ アレクチニブ (Alectinib) [提案 2C]
・ ロルラチニブ (Lorlatinib) [提案 2C]
・ セリチニブ (Ceritinib) [提案 2C]
主要な臨床試験 (PS 0~1)
📊 ALEX試験 [海外]⁴⁾
NEJM. 2017 Aug 31;377(9):829-38.
国際共同無作為化非盲検の第3相試験
前治療歴のないALK陽性進行期NSCLC患者を対象に、 アレクチニブ (600mg 1日2回) とクリゾチニブ (250mg 1日2回)を比較した。 2014年8月~2016年1月の間、 98施設より303例が登録され、 アレクチニブ群 152例、 クリゾチニブ群 151例が無作為に割り付けられた。
無増悪生存期間 [主要評価項目]
- アレクチニブ群 未到達 (95%CI 17.7−NA)
- クリゾチニブ群 11.1ヶ月 (9.1−13.1)
HR 0.47 (0.34−0.65、 P<0.001)
奏功割合
- アレクチニブ群 82.9% (76.0−88.5)
- クリゾチニブ群 75.5% (67.8−82.1)
📊 J-ALEX試験 [国内]⁵⁾⁶⁾
Lancet. 2017 Jul 1;390(10089):29-39. / Lung Cancer. 2020 Jan;139:195-199.
日本人患者対象の第3相試験
日本人進行ALK遺伝子転座陽性非小細胞肺癌患者を対象に、 アレクチニブ (300mg 1日2回) とクリゾチニブ (250mg 1日2回) を比較した。 2013年11月18日~2015年8月4日の間に207例が登録され、 アレクチニブ群 103例、 クリゾチニブ群 104例が無作為に割り付けられた。
無増悪生存期間 [主要評価項目 最終解析]
- アレクチニブ群 34.1ヶ月 (20.3−NA)
- クリゾチニブ群 10.2ヶ月 (8.2-12.0)
HR 0.37 (0.26-0.52、 P<0.001)
奏功割合
- アレクチニブ群 92% (85.6-97.5)
- クリゾチニブ群 79% (70.5-87.3)
主要な臨床試験 (PS 2~4)
📊LOGiK1401試験 [国内]⁷⁾⁸⁾
ALK融合遺伝子陽性のPS不良患者を対象として、 アレクチニブ単剤療法の有効性および安全性を評価した第Ⅱ相試験。 対象患者は計18例 (PS2: 12例、 PS3: 5例、 PS4: 1例)。 有効性は以下のとおりで、 安全性に大きな問題はなかった。
- ORR (主要評価項目) 72.2%
- 無増悪生存期間 [最終解析] 16.2カ月
- OS中央値 [最終解析] 30.3カ月
- PSの改善 83.3%の患者で認めた
参考文献
1) 中外製薬株式会社 「アレセンサ®適正使用ガイド」 (2020年2月改訂) [最終確認 2024/03/02]
2) 日本肺癌学会バイオマーカー委員会. 肺癌患者におけるALK融合遺伝子検査の手引き第4.0版
3) 日本肺癌学会. 肺癌診療ガイドライン−悪性胸膜中皮腫・ 胸腺腫瘍含む−2023年版
最終更新日:2024年3月2日
HOKUTO編集部医師監修
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
