Pemigatinib
ペミガチニブ (ペマジール®)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*インサイト・バイオサイエンシズ・ジャパン合同会社の外部サイトへ遷移します
用法用量
電子添文¹⁾ / 適正使用ガイド²⁾

ペマジール®電子添文 (2023年10月改訂 第5版) 、 適正使用ガイド (2023年3月作成) より作図
1日1回13.5mgを14日間経口投与した後、 7日間休薬
投与開始基準
FIGHT-202試験¹⁾
局所進行性または転移性の胆管癌の組織学的または細胞学的診断ある18歳以上の患者で以下を満たすもの
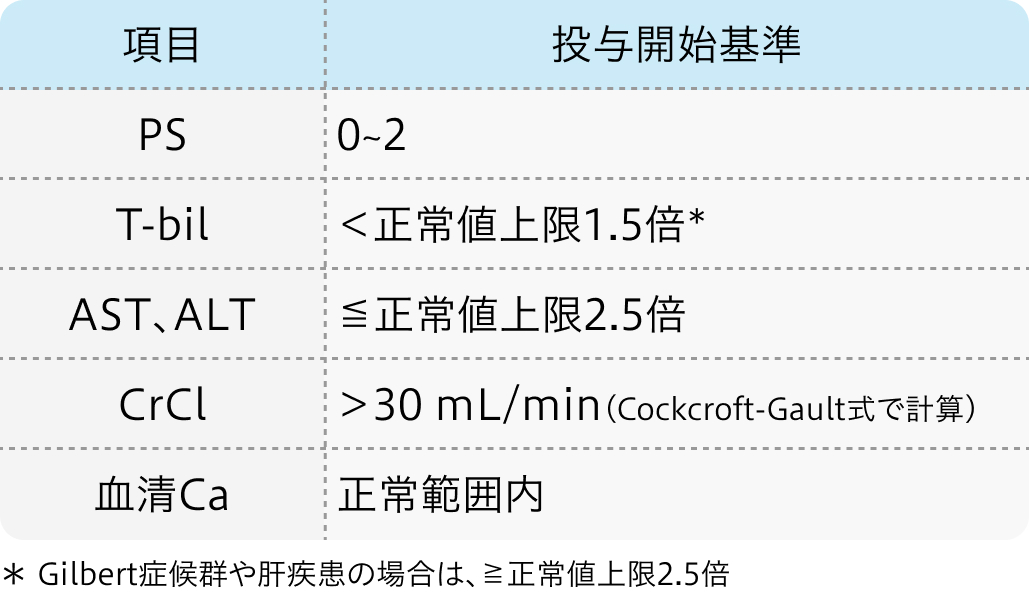
Lancet Oncol. 2020 May;21(5):671-684.より作図
減量・休薬・中止基準
適正使用ガイド²⁾
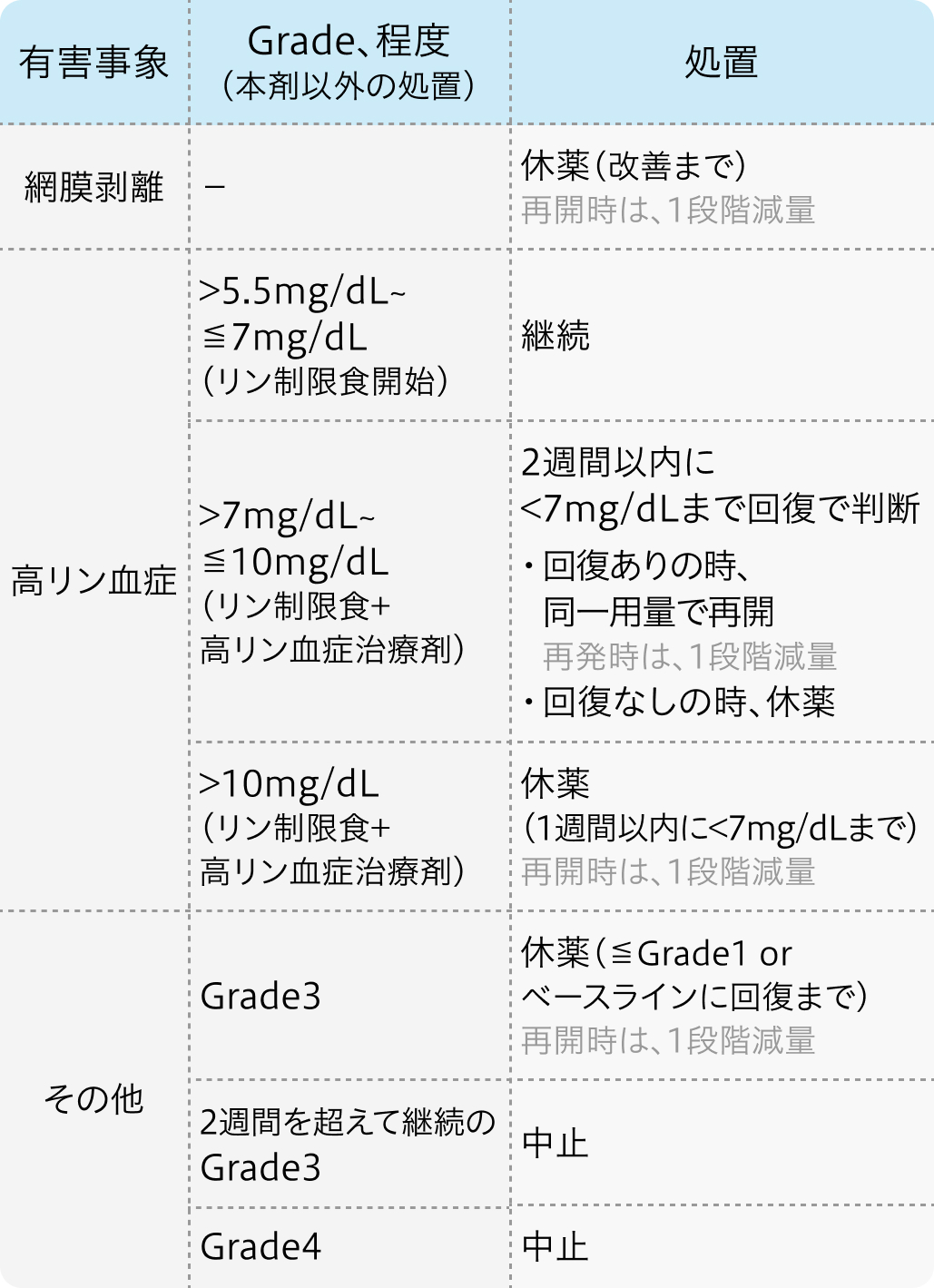
ペマジール®適正使用ガイド (2023年3月作成) より作図
初回基準量と減量レベル

ペマジール®適正使用ガイド (2023年3月作成) より作図
主な有害事象
FIGHT-202試験³⁾
主な有害事象 (カッコ内は≧Grade3)
- 貧血 6.2% (0.7%)
- 下痢 36.3% (2.7%)
- 倦怠感 32.2% (1.4%)
- 口内炎 32.2% (5.5%)
- 吐き気 24.7% (1.4%)
- 食欲減退 24.0% (0.7%)
- 便秘 13.7% (0%)
- 嘔吐 9.6% (0.7%)
注意すべき有害事象 (カッコ内は≧Grade3)
- 脱毛症 45.9% (0%)
- 手掌足底赤血球感覚異常 15.1% (4.1%)
- タンパク尿 0.7% (0.7%)
- 高リン血症 55.5% (0%)
- 角膜炎 2.1% (0.7%)
- 爪障害 22.6% (2.7%)
- 爪変色 7.5% (0.7%)
- 爪白癬 6.2% (0.7%)
- 爪囲炎 6.2% (0.7%)
- その他 2.7% (0.7%)
Lancet Oncol. 2020 May;21(5):671-684.より引用
特徴と注意点
遺伝子変異の検出は稀
本薬剤が有効なFGFR2融合遺伝子の発現頻度は、 本邦では肝内胆管癌の5.3-13.6%、 肝門部領域胆管癌では3.6%と報告されており稀少フラクションである⁴⁻⁶⁾。 遺伝子変異を検出するために積極的ながん遺伝子診断検査の活用が必要である。
高リン血症が多い
本薬剤は国際共同第II相試験のFIGHT-202試験において有効性の検討が行われており、 主要評価項目である奏効割合は35.5%であった。 高リン血症が起こりやすく、 定期的な血液検査と、 検査結果に応じた適切な患者指導、 休薬・減量等を行う。 その他、 脱毛症、 味覚異常、 下痢等の有害事象が起こりやすい。
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
上手に使うためのワンポイント
リン酸を多く含む食品を控える
高リン血症が50.5%に出現することが報告されており、 リン酸を多く含む食品 (インスタント食品、 ナッツ類、 レバー、 加工食品等) を控えるように患者指導し、 血液検査で定期的な血清リン値を確認する。 必要時は高リン血症治療薬 (炭酸ランタン等) の内服を開始し、 適宜休薬、 減量も検討する。
網膜剥離への適切な対応
重大な副作用として網膜剥離 (6.1%) が報告されており、 定期的な眼科受診を行う。 飛蚊症、 視野欠損、 光視症、 視力低下等が認められた場合には、 眼科受診や投与中止等の適切な対処を行う。
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
関連する臨床試験|FIGHT-202試験³⁾
化学療法歴のある切除不能な胆管癌患者において、 FGFR遺伝子に対する選択的阻害薬ペミガチニブの効果を検証した単群コホートの第Ⅱ相試験FIGHT-202の結果より、 FGFR2遺伝子の融合または再構成を有する場合にペミガチニブが有効である可能性が示された。
ORR
- コホートA : 35.5%
(95%CI 26·5-45·4%)
- コホートB : 0%
- コホートC : 0%
病勢コントロール率
- コホートA : 82%
(95%CI 74-89%)
- コホートB : 40%
(95%CI 19-64%)
- コホートC : 22%
(95%CI 6-48%)
奏効期間 (中央値)
- コホートA : 7.5ヵ月
(95%CI 5.7-14.5ヵ月)
PFS中央値
- コホートA : 6.9ヵ月
(95%CI 6.2-9.6ヵ月)
- コホートB : 2.1ヵ月
(95%CI 1.2-4.9ヵ月)
- コホートC : 1.7ヵ月
(95%CI 1.3-1.8ヵ月)
PFS率 (6ヵ月時、 12ヵ月時)
- コホートA : 62%、 29%
- コホートB : 25%、 0%
- コホートC : 6%、 0%
OS中央値
- コホートA : 21.1ヵ月
(95%CI 14.8ヵ月-NE)
- コホートB : 6.7ヵ月
(95%CI 2.1-10.6ヵ月)
- コホートC : 4.0ヵ月
(95%CI 2.3-6.5ヵ月)
OS率 (6ヵ月時、 12ヵ月時)
- コホートA : 89%、 68%
- コホートB : 51%、 23%
- コホートC : 31%、 13%
出典
- インサイト・バイオサイエンシズ・ジャパン合同会社. ペマジール®電子添文 (2023年10月改訂 第5版) [最終閲覧 : 2024/03/22]
- インサイト・バイオサイエンシズ・ジャパン合同会社. ペマジール®適正使用ガイド (2023年3月作成) [最終閲覧 : 2024/03/22]
- Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol. 2020 May;21(5):671-684. PMID: 32203698
- Fibroblast growth factor receptor 2 tyrosine kinase fusions define a unique molecular subtype of cholangiocarcinoma. Hepatology. 2014 Apr;59(4):1427-34. PMID: 24122810
- Molecular detection and clinicopathological characteristics of advanced/recurrent biliary tract carcinomas harboring the FGFR2 rearrangements: a prospective observational study (PRELUDE Study). J Gastroenterol. 2021 Mar;56(3):250-260. PMID: 331069
- Fibroblast growth factor receptor 2 (FGFR2) fusions in Japanese patients with intrahepatic cholangiocarcinoma.Jpn J Clin Oncol. 2021 May 28;51(6):911-917. PMID: 33822966
最終更新日 : 2024年3月22日
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
監修医 : 神奈川県立がんセンター 消化器内科 上野 誠先生
Pemigatinib
Pemigatinib:ペミガチニブ(ペマジール®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 13.5mg/日 経口 分1 | 1~ | Day1~14 |
その他
| 1コース21日間。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*インサイト・バイオサイエンシズ・ジャパン合同会社の外部サイトへ遷移します
用法用量
電子添文¹⁾ / 適正使用ガイド²⁾

ペマジール®電子添文 (2023年10月改訂 第5版) 、 適正使用ガイド (2023年3月作成) より作図
1日1回13.5mgを14日間経口投与した後、 7日間休薬
投与開始基準
FIGHT-202試験¹⁾
局所進行性または転移性の胆管癌の組織学的または細胞学的診断ある18歳以上の患者で以下を満たすもの

Lancet Oncol. 2020 May;21(5):671-684.より作図
減量・休薬・中止基準
適正使用ガイド²⁾

ペマジール®適正使用ガイド (2023年3月作成) より作図
初回基準量と減量レベル

ペマジール®適正使用ガイド (2023年3月作成) より作図
主な有害事象
FIGHT-202試験³⁾
主な有害事象 (カッコ内は≧Grade3)
- 貧血 6.2% (0.7%)
- 下痢 36.3% (2.7%)
- 倦怠感 32.2% (1.4%)
- 口内炎 32.2% (5.5%)
- 吐き気 24.7% (1.4%)
- 食欲減退 24.0% (0.7%)
- 便秘 13.7% (0%)
- 嘔吐 9.6% (0.7%)
注意すべき有害事象 (カッコ内は≧Grade3)
- 脱毛症 45.9% (0%)
- 手掌足底赤血球感覚異常 15.1% (4.1%)
- タンパク尿 0.7% (0.7%)
- 高リン血症 55.5% (0%)
- 角膜炎 2.1% (0.7%)
- 爪障害 22.6% (2.7%)
- 爪変色 7.5% (0.7%)
- 爪白癬 6.2% (0.7%)
- 爪囲炎 6.2% (0.7%)
- その他 2.7% (0.7%)
Lancet Oncol. 2020 May;21(5):671-684.より引用
特徴と注意点
遺伝子変異の検出は稀
本薬剤が有効なFGFR2融合遺伝子の発現頻度は、 本邦では肝内胆管癌の5.3-13.6%、 肝門部領域胆管癌では3.6%と報告されており稀少フラクションである⁴⁻⁶⁾。 遺伝子変異を検出するために積極的ながん遺伝子診断検査の活用が必要である。
高リン血症が多い
本薬剤は国際共同第II相試験のFIGHT-202試験において有効性の検討が行われており、 主要評価項目である奏効割合は35.5%であった。 高リン血症が起こりやすく、 定期的な血液検査と、 検査結果に応じた適切な患者指導、 休薬・減量等を行う。 その他、 脱毛症、 味覚異常、 下痢等の有害事象が起こりやすい。
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
上手に使うためのワンポイント
リン酸を多く含む食品を控える
高リン血症が50.5%に出現することが報告されており、 リン酸を多く含む食品 (インスタント食品、 ナッツ類、 レバー、 加工食品等) を控えるように患者指導し、 血液検査で定期的な血清リン値を確認する。 必要時は高リン血症治療薬 (炭酸ランタン等) の内服を開始し、 適宜休薬、 減量も検討する。
網膜剥離への適切な対応
重大な副作用として網膜剥離 (6.1%) が報告されており、 定期的な眼科受診を行う。 飛蚊症、 視野欠損、 光視症、 視力低下等が認められた場合には、 眼科受診や投与中止等の適切な対処を行う。
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
関連する臨床試験|FIGHT-202試験³⁾
化学療法歴のある切除不能な胆管癌患者において、 FGFR遺伝子に対する選択的阻害薬ペミガチニブの効果を検証した単群コホートの第Ⅱ相試験FIGHT-202の結果より、 FGFR2遺伝子の融合または再構成を有する場合にペミガチニブが有効である可能性が示された。
ORR
- コホートA : 35.5%
(95%CI 26·5-45·4%)
- コホートB : 0%
- コホートC : 0%
病勢コントロール率
- コホートA : 82%
(95%CI 74-89%)
- コホートB : 40%
(95%CI 19-64%)
- コホートC : 22%
(95%CI 6-48%)
奏効期間 (中央値)
- コホートA : 7.5ヵ月
(95%CI 5.7-14.5ヵ月)
PFS中央値
- コホートA : 6.9ヵ月
(95%CI 6.2-9.6ヵ月)
- コホートB : 2.1ヵ月
(95%CI 1.2-4.9ヵ月)
- コホートC : 1.7ヵ月
(95%CI 1.3-1.8ヵ月)
PFS率 (6ヵ月時、 12ヵ月時)
- コホートA : 62%、 29%
- コホートB : 25%、 0%
- コホートC : 6%、 0%
OS中央値
- コホートA : 21.1ヵ月
(95%CI 14.8ヵ月-NE)
- コホートB : 6.7ヵ月
(95%CI 2.1-10.6ヵ月)
- コホートC : 4.0ヵ月
(95%CI 2.3-6.5ヵ月)
OS率 (6ヵ月時、 12ヵ月時)
- コホートA : 89%、 68%
- コホートB : 51%、 23%
- コホートC : 31%、 13%
出典
- インサイト・バイオサイエンシズ・ジャパン合同会社. ペマジール®電子添文 (2023年10月改訂 第5版) [最終閲覧 : 2024/03/22]
- インサイト・バイオサイエンシズ・ジャパン合同会社. ペマジール®適正使用ガイド (2023年3月作成) [最終閲覧 : 2024/03/22]
- Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol. 2020 May;21(5):671-684. PMID: 32203698
- Fibroblast growth factor receptor 2 tyrosine kinase fusions define a unique molecular subtype of cholangiocarcinoma. Hepatology. 2014 Apr;59(4):1427-34. PMID: 24122810
- Molecular detection and clinicopathological characteristics of advanced/recurrent biliary tract carcinomas harboring the FGFR2 rearrangements: a prospective observational study (PRELUDE Study). J Gastroenterol. 2021 Mar;56(3):250-260. PMID: 331069
- Fibroblast growth factor receptor 2 (FGFR2) fusions in Japanese patients with intrahepatic cholangiocarcinoma.Jpn J Clin Oncol. 2021 May 28;51(6):911-917. PMID: 33822966
最終更新日 : 2024年3月22日
執筆医 : 北海道大学病院 腫瘍センター 助教 川本 泰之先生
監修医 : 神奈川県立がんセンター 消化器内科 上野 誠先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
