DTX+DAR
ドセタキセル (ワンタキソテール®)+ダロタミド
DTX:ドセタキセル(ワンタキソテール®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 75mg/m² 点滴 | 1~ | Day1 |
DAR:ダロルタミド(ニュベクオ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1200mg/日 1日2回 経口投与 | 連日服用 | Day1 |
その他
| 1コース21日間 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*サノフィ株式会社の外部サイトへ遷移します
*バイエル薬品株式会社の外部サイトへ遷移します
用法用量
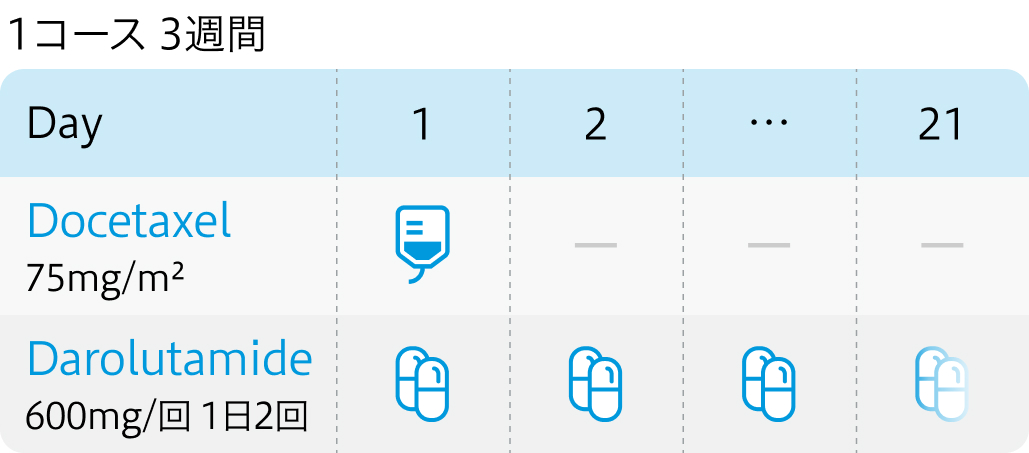
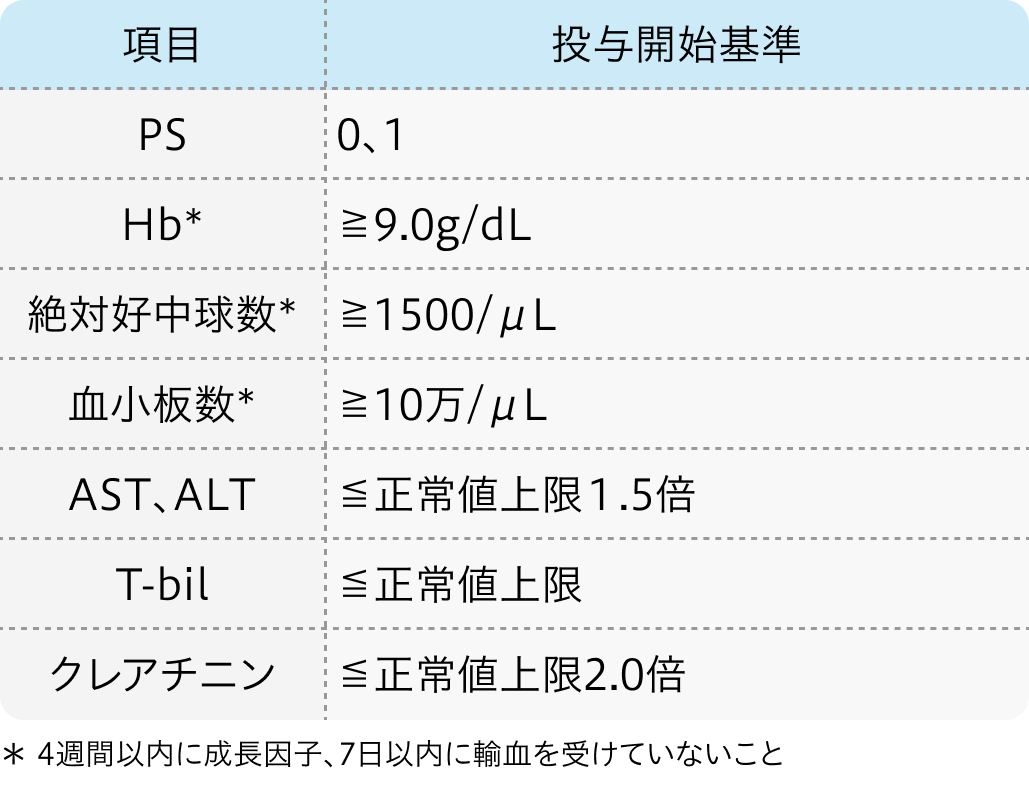
投与開始基準
ARASENS試験¹⁾より抜粋
減量・延期・休薬・中止基準
ドセタキセルの延期基準
- ビリルビン:>正常値上限
- AST及び / 又はALT:>正常値上限の1.5倍
ドセタキセルの減量・中止基準
以下の場合、 75mg/m²ら60mg/m²に減量。 減量後も持続する場合、 ドセタキセル投与中止
- 発熱性好中球減少症
- <500/mm³の好中球数が1週間を超えて持続
- 重度又は累積的皮膚反応
- 重度末梢性ニューロパチー
ダロルタミドの減量・休薬基準
Grade3以上又は忍容できない副作用があらわれた場合、 回復するまで休薬。
回復後、 1回300mg1日2回に減量で再開を考慮。
患者の状態により、 通常用量に増量も可
主な有害事象
ARASENS試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 貧血 28.4% (4.8%)
- 好中球数減少 26.2% (23.3%)
- 白血球数減少 23.8% (16.9%)
- ALT増加 15.8% (2.8%)
- 疲労 33.9% (1.7%)
- 下痢 25.9% (1.2%)
- 便秘 22.9% (0.3%)
- 食欲減退 18.6% (0.2%)
- 悪心 17.9% (0.5%)
- 体重増加 17.8% (2.1%)
- 体重減少 3.7% (0%)
注意すべき有害事象
- 脱毛症 40.8% (0.2%)
- 糖尿病・高血糖 15.3% (3.7%)
- 高血圧 13.8% (6.7%)
特徴と注意点
ADT開始後12週以内にダロルタミドを開始する。
ダロルタミド開始後6週以内にDTXを開始する。
DTXは6サイクルで終了
関連する臨床試験|ARASENS試験¹⁾
転移性ホルモン感受性前立腺癌患者において、 アンドロゲン除去療法 (ADT) +ドセタキセル (DTX) にダロルタミドを併用する効果を、 プラセボを対照に検証した第Ⅲ相比較試験ARASENSの結果より、 全生存期間 (OS) に対する有益性が示された。
OS
- ダロルタミド群において、 OSの有意な延長がみられた。
HR 0.68 (95%CI 0.57-0.80)、 P<0.001
- 4年時のOS率は、 ダロルタミド群で62.7% (95%CI 58.7-66.7) 、 プラセボ群で50.4% (95%CI 46.3-54.6) であった。
OSのサブグループ解析
年齢や人種などの事前に規定された全てのサブグループにおいて、 ハザード比の点推定値が1を下回った。
去勢抵抗性前立腺癌となるまでの期間
HR 0.36 (95%CI 0.30-0.42)、 P<0.001
疼痛増悪までの期間
HR 0.79 (95%CI 0.66-0.95)、P=0.01
SSE無発症生存期間
HR 0.61 (95%CI 0.52-0.72)、 P<0.001
SSEの初回発現までの期間
HR 0.71 (95%CI 0.54-0.94)、 P=0.02
後治療開始までの期間
HR 0.39 (95%CI 0.33-0.46)、 P<0.001
参考文献
最終更新日:2023年11月21日
監修医師:国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
DTX+DAR
DTX:ドセタキセル(ワンタキソテール®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 75mg/m² 点滴 | 1~ | Day1 |
DAR:ダロルタミド(ニュベクオ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1200mg/日 1日2回 経口投与 | 連日服用 | Day1 |
その他
| 1コース21日間 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*サノフィ株式会社の外部サイトへ遷移します
*バイエル薬品株式会社の外部サイトへ遷移します
用法用量

投与開始基準
ARASENS試験¹⁾より抜粋

減量・延期・休薬・中止基準
ドセタキセルの延期基準
- ビリルビン:>正常値上限
- AST及び / 又はALT:>正常値上限の1.5倍
ドセタキセルの減量・中止基準
以下の場合、 75mg/m²ら60mg/m²に減量。 減量後も持続する場合、 ドセタキセル投与中止
- 発熱性好中球減少症
- <500/mm³の好中球数が1週間を超えて持続
- 重度又は累積的皮膚反応
- 重度末梢性ニューロパチー
ダロルタミドの減量・休薬基準
Grade3以上又は忍容できない副作用があらわれた場合、 回復するまで休薬。
回復後、 1回300mg1日2回に減量で再開を考慮。
患者の状態により、 通常用量に増量も可
主な有害事象
ARASENS試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 貧血 28.4% (4.8%)
- 好中球数減少 26.2% (23.3%)
- 白血球数減少 23.8% (16.9%)
- ALT増加 15.8% (2.8%)
- 疲労 33.9% (1.7%)
- 下痢 25.9% (1.2%)
- 便秘 22.9% (0.3%)
- 食欲減退 18.6% (0.2%)
- 悪心 17.9% (0.5%)
- 体重増加 17.8% (2.1%)
- 体重減少 3.7% (0%)
注意すべき有害事象
- 脱毛症 40.8% (0.2%)
- 糖尿病・高血糖 15.3% (3.7%)
- 高血圧 13.8% (6.7%)
特徴と注意点
ADT開始後12週以内にダロルタミドを開始する。
ダロルタミド開始後6週以内にDTXを開始する。
DTXは6サイクルで終了
関連する臨床試験|ARASENS試験¹⁾
転移性ホルモン感受性前立腺癌患者において、 アンドロゲン除去療法 (ADT) +ドセタキセル (DTX) にダロルタミドを併用する効果を、 プラセボを対照に検証した第Ⅲ相比較試験ARASENSの結果より、 全生存期間 (OS) に対する有益性が示された。
OS
- ダロルタミド群において、 OSの有意な延長がみられた。
HR 0.68 (95%CI 0.57-0.80)、 P<0.001
- 4年時のOS率は、 ダロルタミド群で62.7% (95%CI 58.7-66.7) 、 プラセボ群で50.4% (95%CI 46.3-54.6) であった。
OSのサブグループ解析
年齢や人種などの事前に規定された全てのサブグループにおいて、 ハザード比の点推定値が1を下回った。
去勢抵抗性前立腺癌となるまでの期間
HR 0.36 (95%CI 0.30-0.42)、 P<0.001
疼痛増悪までの期間
HR 0.79 (95%CI 0.66-0.95)、P=0.01
SSE無発症生存期間
HR 0.61 (95%CI 0.52-0.72)、 P<0.001
SSEの初回発現までの期間
HR 0.71 (95%CI 0.54-0.94)、 P=0.02
後治療開始までの期間
HR 0.39 (95%CI 0.33-0.46)、 P<0.001
参考文献
最終更新日:2023年11月21日
監修医師:国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
