Nivo
ニボルマブ
Nivo:ニボルマブ(オプジーボ®)
| 投与量 | コース | 投与日 |
|---|---|---|
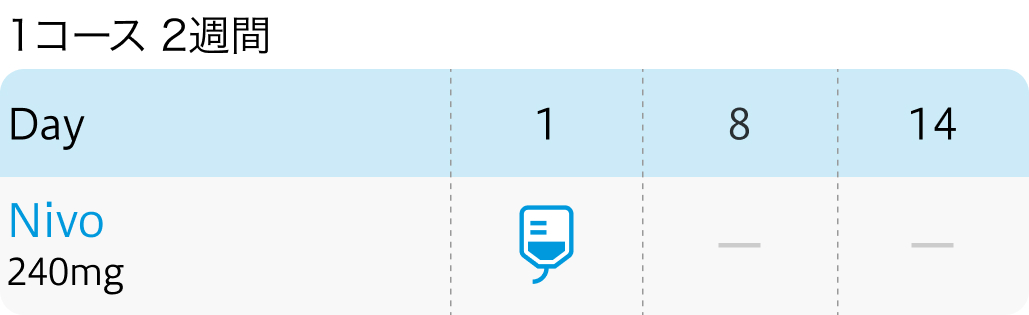
| 240mg/body 点滴 (2週間) | 1~ | Day1 |
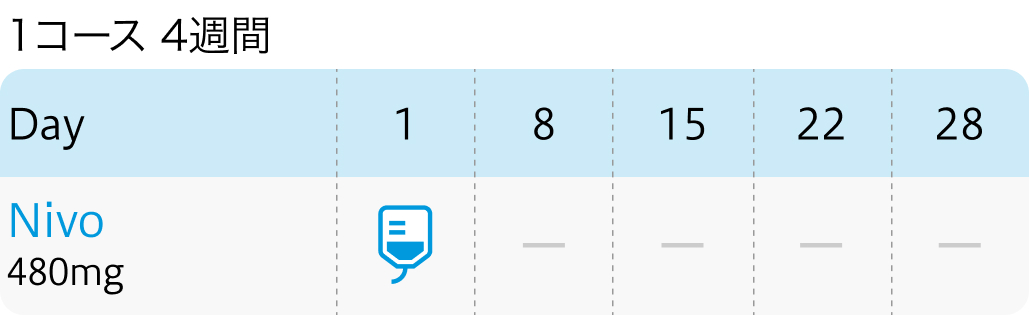
| 480mg/body 点滴 (4週間) | 1~ | Day1 |
その他
| 1コース14日間もしくは28日間 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*小野薬品工業の外部サイトへ遷移します
用法用量 (1コース2週間、 4週間)
投与開始基準
CheckMate 025試験の基準より抜粋¹⁾
未治療の淡明細胞型腎細胞がんの組織学的または細胞学的診断ある18歳以上 での患者でKPSが≧70%の患者
減量基準
ニボルマブの減量はできない
中止基準
CheckMate 025試験の基準より抜粋¹⁾
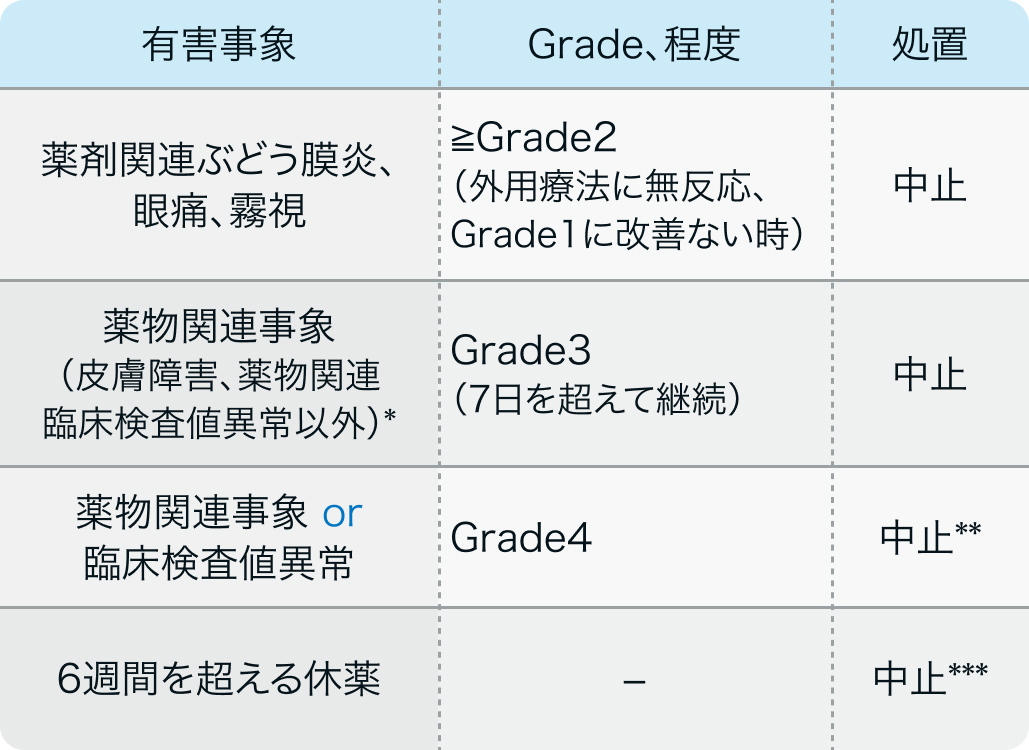
*以下の場合は中止
薬物関連血小板減少症が7日以上継続か、出血を伴う場合
薬物関連肝機能検査異常で、 以下の条件に当てはまる場合
- ASTまたはALT:>基準値上限の5~10倍が2週間超持続
- ASTまたはALT:>基準値上限の10倍
- T-bil: >基準値上限の5倍
- ASTまたはALTが基準値上限の3倍かつT-bilが基準値上限の2倍
薬物関連気管支痙攣、 過敏症反応、 infusion reaction、 ぶどう膜炎、 肺炎
**以下の場合は中止しない
- 7日以内の好中球減少症
- リンパ球減少症
- 白血球減少症
- 臨床症状を伴わず、 発症から72時間以内に補充・適切な管理で改善される単発の電解質異常/平衡失調症
***以下の場合を除く
- 薬物関連有害事象の管理のためのステロイドの漸減が長期化するための休薬
- 薬剤の関連がない6週間を超える休薬は再開の検討が可能
主な有害事象
CheckMate 025試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感 33.0% (2.5%)
- 悪心 14.0% (0.2%)
- 下痢 12.3% (1.2%)
- 食欲低下 11.8% (0.5%)
- 貧血 78.8% (1.7%)
- 粘膜炎症 2.7% (0%)
- 口内炎 2.0% (0%)
注意すべき有害事象
- 高血糖 2.2% (1.2%)
- 高トリグリセリド血症 1.2% (0%)
特徴と注意点
血管新生阻害薬2剤目以降においてエベロリムスとの比較でOSを改善したレジメンである。
すべてのIMDCリスクの症例に適用可能
関連する臨床試験|CheckMate 025試験¹⁾
血管新生阻害剤での治療歴を有する進行性または転移性腎細胞癌患者において、 ニボルマブ投与の効果を、 エベロリムス投与を対照に検証した比較試験CheckMate 025の結果より、 全生存期間 (OS) 、 無増悪生存期間 (PFS) 、 奏効率 (ORR) に対する有益性が示された。
OS
- 中央値
- ニボルマブ群:25.8ヵ月
(95%CI 22.2-29.8ヵ月)
- エベロリムス群:19.7ヵ月
(95%CI 17.6-22.1ヵ月)
HR0.73 (95%CI 0.62-0.85)、 p<0.0001
- 3年時、 4年時、 5年時のOS率
- ニボルマブ群:39%、 30%、 26%
- エベロリムス群:30%、 23%、 18%
PFS中央値
- 中央値
- ニボルマブ群:4.2ヵ月
(95%CI 3.7-5.4ヵ月)
- エベロリムス群:4.5ヵ月
(95%CI 3.7-5.5ヵ月)
HR 0.84 (95%CI 0.72-0.99)、 P=0.0331
- 3年時、 4年時、 5年時のPFS率
- ニボルマブ群:9%、 6%、 5%
- エベロリムス群:2%、 1%、 1%
OSとPD-L1発現との関連 (初回報告のみで評価)
PD-L1発現を評価できたのは、 ニボルマブ群370例 (90%) 、 エベロリムス群386例 (94%) であった。
- PD-L1発現が1%以上の患者のOS中央値 181/756例 (24%)
- ニボルマブ群:21.8ヵ月
(95%CI 16.5-28.1ヵ月)
- エベロリムス群:18.8ヵ月
(95%CI 11.9-19.9ヵ月)
HR 0.78 (95%CI 0.53-1.16)
- PD-L1発現が1%未満の患者のOS中央値 575/756例 (76%)
- ニボルマブ群:27.4ヵ月
(95%CI 21.4ヵ月-推定不能)
- エベロリムス群:21.2ヵ月
(95%CI 17.7ヵ月-26.2ヵ月)
HR 0.76 (95%CI 0.60-0.97)
ORR
- ニボルマブ群:22.9%
(95%CI 18.9-27.3%)
- エベロリムス群:4.1%
(95%CI 2.4-6.5%)
オッズ比 6.86 (95%CI 4.0-11.7)、 P<0.0001
奏効までの期間 (中央値)
- ニボルマブ群:3.5ヵ月
- エベロリムス群:3.7ヵ月
奏効期間 (中央値)
- ニボルマブ群:18.2ヵ月
(95%CI 12.9-25.8ヵ月)
- エベロリムス群:14.0ヵ月
(95%CI 8.3-19.2ヵ月)
参考文献
最終更新日:2023年10月20日
監修医師:国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
Nivo
Nivo:ニボルマブ(オプジーボ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 240mg/body 点滴 (2週間) | 1~ | Day1 |
| 480mg/body 点滴 (4週間) | 1~ | Day1 |
その他
| 1コース14日間もしくは28日間 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*小野薬品工業の外部サイトへ遷移します
用法用量 (1コース2週間、 4週間)


投与開始基準
CheckMate 025試験の基準より抜粋¹⁾
未治療の淡明細胞型腎細胞がんの組織学的または細胞学的診断ある18歳以上 での患者でKPSが≧70%の患者
減量基準
ニボルマブの減量はできない
中止基準
CheckMate 025試験の基準より抜粋¹⁾

*以下の場合は中止
薬物関連血小板減少症が7日以上継続か、出血を伴う場合
薬物関連肝機能検査異常で、 以下の条件に当てはまる場合
- ASTまたはALT:>基準値上限の5~10倍が2週間超持続
- ASTまたはALT:>基準値上限の10倍
- T-bil: >基準値上限の5倍
- ASTまたはALTが基準値上限の3倍かつT-bilが基準値上限の2倍
薬物関連気管支痙攣、 過敏症反応、 infusion reaction、 ぶどう膜炎、 肺炎
**以下の場合は中止しない
- 7日以内の好中球減少症
- リンパ球減少症
- 白血球減少症
- 臨床症状を伴わず、 発症から72時間以内に補充・適切な管理で改善される単発の電解質異常/平衡失調症
***以下の場合を除く
- 薬物関連有害事象の管理のためのステロイドの漸減が長期化するための休薬
- 薬剤の関連がない6週間を超える休薬は再開の検討が可能
主な有害事象
CheckMate 025試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感 33.0% (2.5%)
- 悪心 14.0% (0.2%)
- 下痢 12.3% (1.2%)
- 食欲低下 11.8% (0.5%)
- 貧血 78.8% (1.7%)
- 粘膜炎症 2.7% (0%)
- 口内炎 2.0% (0%)
注意すべき有害事象
- 高血糖 2.2% (1.2%)
- 高トリグリセリド血症 1.2% (0%)
特徴と注意点
血管新生阻害薬2剤目以降においてエベロリムスとの比較でOSを改善したレジメンである。
すべてのIMDCリスクの症例に適用可能
関連する臨床試験|CheckMate 025試験¹⁾
血管新生阻害剤での治療歴を有する進行性または転移性腎細胞癌患者において、 ニボルマブ投与の効果を、 エベロリムス投与を対照に検証した比較試験CheckMate 025の結果より、 全生存期間 (OS) 、 無増悪生存期間 (PFS) 、 奏効率 (ORR) に対する有益性が示された。
OS
- 中央値
- ニボルマブ群:25.8ヵ月
(95%CI 22.2-29.8ヵ月)
- エベロリムス群:19.7ヵ月
(95%CI 17.6-22.1ヵ月)
HR0.73 (95%CI 0.62-0.85)、 p<0.0001
- 3年時、 4年時、 5年時のOS率
- ニボルマブ群:39%、 30%、 26%
- エベロリムス群:30%、 23%、 18%
PFS中央値
- 中央値
- ニボルマブ群:4.2ヵ月
(95%CI 3.7-5.4ヵ月)
- エベロリムス群:4.5ヵ月
(95%CI 3.7-5.5ヵ月)
HR 0.84 (95%CI 0.72-0.99)、 P=0.0331
- 3年時、 4年時、 5年時のPFS率
- ニボルマブ群:9%、 6%、 5%
- エベロリムス群:2%、 1%、 1%
OSとPD-L1発現との関連 (初回報告のみで評価)
PD-L1発現を評価できたのは、 ニボルマブ群370例 (90%) 、 エベロリムス群386例 (94%) であった。
- PD-L1発現が1%以上の患者のOS中央値 181/756例 (24%)
- ニボルマブ群:21.8ヵ月
(95%CI 16.5-28.1ヵ月)
- エベロリムス群:18.8ヵ月
(95%CI 11.9-19.9ヵ月)
HR 0.78 (95%CI 0.53-1.16)
- PD-L1発現が1%未満の患者のOS中央値 575/756例 (76%)
- ニボルマブ群:27.4ヵ月
(95%CI 21.4ヵ月-推定不能)
- エベロリムス群:21.2ヵ月
(95%CI 17.7ヵ月-26.2ヵ月)
HR 0.76 (95%CI 0.60-0.97)
ORR
- ニボルマブ群:22.9%
(95%CI 18.9-27.3%)
- エベロリムス群:4.1%
(95%CI 2.4-6.5%)
オッズ比 6.86 (95%CI 4.0-11.7)、 P<0.0001
奏効までの期間 (中央値)
- ニボルマブ群:3.5ヵ月
- エベロリムス群:3.7ヵ月
奏効期間 (中央値)
- ニボルマブ群:18.2ヵ月
(95%CI 12.9-25.8ヵ月)
- エベロリムス群:14.0ヵ月
(95%CI 8.3-19.2ヵ月)
参考文献
最終更新日:2023年10月20日
監修医師:国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

