adj. Nivo
Nivo (オプジーボ®)
治療スケジュール
概要
監修医師
Nivo:ニボルマブ(オプジーボ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 240mg/body 点滴 (2週間) | 1~ | Day1 |
| 480mg/body 点滴 (4週間) | 1~ | Day1 |
前投薬
| infusion reactionが生じた場合、 ステロイドや抗ヒスタミンなどを考慮する。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*小野薬品工業の外部サイトへ遷移します
用法用量 (1コース2週間 or 4週間)
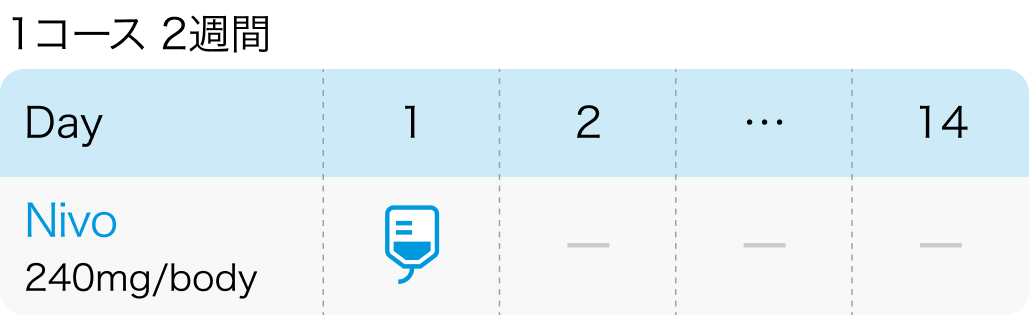

前投薬
infusion reactionが生じた場合、 ステロイドや抗ヒスタミンなどを考慮する。
投与開始基準
CheckMate 577試験¹⁾の基準より抜粋
18歳以上で食道癌または胃食道接合部癌を切除し、 術前補助化学放射線療法を受けたPS0~1の患者
主な有害事象
CheckMate 577試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感 16.9% (1.1%)
- 下痢 16.5% (0.4%)
- 甲状腺機能低下症 9.4% (0%)
- 悪心 8.8% (0%)
- 甲状腺機能亢進症 6.6% (0%)
- AST増加 5.5% (0.4%)
- 食欲減退 4.9% (0%)
上手に使うためのワンポイント
- 本レジメンの根拠となったCheckMate577試験¹⁾では、 術前CRT後、 病理学的CRとならなかった症例が対象となった。 厳密には術前化学療法後のAdj. Nivoに関しては明確なエビデンスはなく症例に合わせて行われているのが実情である。
- 術前化学療法後のAdj. Nivo、 AdjS-1、 無治療との3群を比較したJCOG2206試験が行われており同試験の結果が待たれる。
- 自己免疫性疾患を有し10mgを超えるプレドニゾロンを内服している症例や免疫調整剤を服用している症例は自己免疫性疾患増悪のリスクがあるため避けるべきである。
特徴と注意点
- irAEに注意が必要であり、 定期的な甲状腺機能や血糖などの内分泌機能、 肝障害、 腎障害のチェック、 SPO₂の測定が必要である。 irAEを来した場合、 甲状腺機能低下症や副腎皮質機能低下症などのホルモン補充で対処可能な内分泌障害は治療継続可能であるが、 それ以外では治療を中断しプレドニゾロンによる治療を要する。irAE後のNivoの再開についてはリスク、 ベネフィットを考慮し慎重に検討する。
- ホルモン補充で対処可能な内分泌障害以外の≧Grade3のirAEに関しては再投与を控える。 肺臓炎に関しては≧Grade2で再投与を控える。
- 食道癌では喫煙歴のある症例が多いためしばしば肺に間質影を伴う症例を経験する。 CT画像で肺底部に間質影が存在しないか注意深く観察する必要がある。
関連する臨床試験|CheckMate 577試験¹⁾
術前化学放射線療法および完全切除後に病理学的残存病変を認めたStageII~IIIの食道/食道胃接合部癌患者において、 術後療法における抗PD-1抗体ニボルマブの効果を、 プラセボを対照に検証した第Ⅲ相二重盲検ランダム化比較試験CheckMate 577の結果より、 無病生存期間 (DFS) に対する有効性が示された。
追跡期間中央値
24.4ヵ月
DFS中央値
- ニボルマブ群:22.4ヵ月
(95%CI 16.6-34.0ヵ月)
- プラセボ群:11.0ヵ月
(95%CI 8.3-14.3ヵ月)
HR 0.69 (96.4%CI 0.56-0.86)、 p<0.001
DFSのサブグループ解析
腫瘍のPD-L1発現量に関わらず、 HRはニボルマブ群が有利であった。
DMFS中央値
- ニボルマブ群:28.3ヵ月
(95%CI 21.3ヵ月-NE)
- プラセボ群:17.6ヵ月
(95%CI 12.5-25.4ヵ月)
HR 0.74 (95%CI 0.60-0.92)
患者報告アウトカム
- FACT-E総スコア、 EQ-5D-3L視覚アナログスケール、 およびEQ-5D-3Lの健康ユーティリティスコアにおいて、 最小二乗平均スコアの差を比較
- 53週目までのほぼ全ての時点において、 ニボルマブ群およびプラセボ群の両群でベースラインから同様の改善が示された。
参考文献
最終更新日:2023年11月21日
監修医師:HOKUTO編集部監修医師
adj. Nivo
Nivo (オプジーボ®)
2023年12月12日更新
Nivo:ニボルマブ(オプジーボ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 240mg/body 点滴 (2週間) | 1~ | Day1 |
| 480mg/body 点滴 (4週間) | 1~ | Day1 |
前投薬
| infusion reactionが生じた場合、 ステロイドや抗ヒスタミンなどを考慮する。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*小野薬品工業の外部サイトへ遷移します
用法用量 (1コース2週間 or 4週間)


前投薬
infusion reactionが生じた場合、 ステロイドや抗ヒスタミンなどを考慮する。
投与開始基準
CheckMate 577試験¹⁾の基準より抜粋
18歳以上で食道癌または胃食道接合部癌を切除し、 術前補助化学放射線療法を受けたPS0~1の患者
主な有害事象
CheckMate 577試験¹⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感 16.9% (1.1%)
- 下痢 16.5% (0.4%)
- 甲状腺機能低下症 9.4% (0%)
- 悪心 8.8% (0%)
- 甲状腺機能亢進症 6.6% (0%)
- AST増加 5.5% (0.4%)
- 食欲減退 4.9% (0%)
上手に使うためのワンポイント
- 本レジメンの根拠となったCheckMate577試験¹⁾では、 術前CRT後、 病理学的CRとならなかった症例が対象となった。 厳密には術前化学療法後のAdj. Nivoに関しては明確なエビデンスはなく症例に合わせて行われているのが実情である。
- 術前化学療法後のAdj. Nivo、 AdjS-1、 無治療との3群を比較したJCOG2206試験が行われており同試験の結果が待たれる。
- 自己免疫性疾患を有し10mgを超えるプレドニゾロンを内服している症例や免疫調整剤を服用している症例は自己免疫性疾患増悪のリスクがあるため避けるべきである。
特徴と注意点
- irAEに注意が必要であり、 定期的な甲状腺機能や血糖などの内分泌機能、 肝障害、 腎障害のチェック、 SPO₂の測定が必要である。 irAEを来した場合、 甲状腺機能低下症や副腎皮質機能低下症などのホルモン補充で対処可能な内分泌障害は治療継続可能であるが、 それ以外では治療を中断しプレドニゾロンによる治療を要する。irAE後のNivoの再開についてはリスク、 ベネフィットを考慮し慎重に検討する。
- ホルモン補充で対処可能な内分泌障害以外の≧Grade3のirAEに関しては再投与を控える。 肺臓炎に関しては≧Grade2で再投与を控える。
- 食道癌では喫煙歴のある症例が多いためしばしば肺に間質影を伴う症例を経験する。 CT画像で肺底部に間質影が存在しないか注意深く観察する必要がある。
関連する臨床試験|CheckMate 577試験¹⁾
術前化学放射線療法および完全切除後に病理学的残存病変を認めたStageII~IIIの食道/食道胃接合部癌患者において、 術後療法における抗PD-1抗体ニボルマブの効果を、 プラセボを対照に検証した第Ⅲ相二重盲検ランダム化比較試験CheckMate 577の結果より、 無病生存期間 (DFS) に対する有効性が示された。
追跡期間中央値
24.4ヵ月
DFS中央値
- ニボルマブ群:22.4ヵ月
(95%CI 16.6-34.0ヵ月)
- プラセボ群:11.0ヵ月
(95%CI 8.3-14.3ヵ月)
HR 0.69 (96.4%CI 0.56-0.86)、 p<0.001
DFSのサブグループ解析
腫瘍のPD-L1発現量に関わらず、 HRはニボルマブ群が有利であった。
DMFS中央値
- ニボルマブ群:28.3ヵ月
(95%CI 21.3ヵ月-NE)
- プラセボ群:17.6ヵ月
(95%CI 12.5-25.4ヵ月)
HR 0.74 (95%CI 0.60-0.92)
患者報告アウトカム
- FACT-E総スコア、 EQ-5D-3L視覚アナログスケール、 およびEQ-5D-3Lの健康ユーティリティスコアにおいて、 最小二乗平均スコアの差を比較
- 53週目までのほぼ全ての時点において、 ニボルマブ群およびプラセボ群の両群でベースラインから同様の改善が示された。
参考文献
最終更新日:2023年11月21日
監修医師:HOKUTO編集部監修医師
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(消化器)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

